A molekulák szerkezete és tulajdonságai
Minden körülöttünk lévő testet atomok alkotják. Az atomok pedig molekulákká alakulnak. Pontosan a molekulaszerkezetben rejlő különbségnek köszönhetően egymástól különböző anyagokról beszélhetünk tulajdonságaik és paramétereik alapján. A molekulák és az atomok mindig dinamikus állapotban vannak. A mozgás közben még mindig nem szétszóródnak különböző irányokban, hanem egy bizonyos struktúrában vannak, ami az egész világon olyan nagy mennyiségű anyag létezésének köszönhető. Mik ezek a részecskék és mi a tulajdonsága?
Általános fogalmak
Ha a kvantummechanika elméletéből indulunk ki, akkor a molekula nem atomokból, hanem azok magvából és elektronokból áll, amelyek folyamatosan kölcsönhatásban állnak egymással.
Egyes anyagok esetében a molekula a legkisebbolyan részecske, amely magában az anyag összetételét és kémiai tulajdonságait tartalmazza. Tehát a molekulák tulajdonságait a kémia szempontjából kémiai szerkezete és összetétele határozza meg. De csak a molekulaszerkezetű anyagok esetében működik a szabály: az anyagok és molekulák kémiai tulajdonságai megegyeznek. Egyes polimerek, például etilén és polietilén esetében a készítmény nem felel meg a molekulaszerkezetnek.
Ismeretes, hogy a molekulák tulajdonságait nem határozzák megcsak az atomok száma, típusa, hanem a konfiguráció, a kapcsolat sorrendje. A molekula összetett építészeti struktúra, ahol minden egyes elem a helyén áll és saját szomszédai vannak. Az atomszerkezet többé-kevésbé merev lehet. Minden atom oszcillál az egyensúlyi helyzetéhez képest.

Konfiguráció és paraméterek
Előfordul, hogy a molekula egyes részeinek más részeihez képest forognak. Így a termikus mozgás folyamán a szabad molekula bizarr formákat (konfigurációkat) szerez.
Alapvetően a molekulák tulajdonságait a kötés határozza meg(típusát) az atomok és maga a molekula felépítése (szerkezet, forma) között. Így mindenekelőtt az általános kémiai elmélet vegyi kötéseket tart, és az atomok tulajdonságain alapul.
Kimondott molekulák polaritási tulajdonságaivalNehéz leírni két vagy három állandó összefüggést, amelyek nagyszerűek a nem poláris molekulák számára. Ezért egy további dipólus pillanatnyi paramétert vezettek be. De ez a módszer nem mindig sikeres, mivel a poláris molekulák egyedi tulajdonságokkal rendelkeznek. Paramétereket is javasoltak az alacsony hőmérsékleteken fontos kvantumhatásokra.

Mit tudunk a Föld legáltalánosabb anyagának molekulájáról?
A bolygónk összes anyagáról a legtöbbetközös a víz. Ő, szó szerinti értelemben, életet biztosít a földi dolgoknak. Kizárólag a vírusok képesek megtenni nélküle, a fennmaradó élő struktúrák összetételében nagyrészt vízzel rendelkeznek. Milyen tulajdonságai vannak a vízmolekulának, amely csak azokra jellemző, az ember gazdasági életében és a Föld élő természetében?
Végül is ez valóban egyedülálló anyag! A vízben rejlő tulajdonságok sorozata többé nem büszkélkedhet.
A víz a fő oldószer a természetben. Az élő szervezetekben előforduló összes reakció bármelyik módon fordul elő a vízi környezetben. Vagyis az anyagok reakcióba lépnek, mivel oldott állapotban vannak.
A víz kiváló hő kapacitása, de alacsonyhővezető képesség. Ezeknek a tulajdonságoknak köszönhetően hőt szállíthatjuk. Ez az elv számos nagyszámú szervezet hűtési mechanizmusában szerepel. Az atomi energiában a vízmolekula tulajdonságai voltak az oka annak, hogy ezt az anyagot hűtőfolyadékként használják. Amellett, hogy más anyagok reakcióképes közegét képezheti, maga a víz képes reagálni: fotolízis, hidratálás és mások.

A természetes tiszta víz folyadék, szagtalan, színtelen és íztelen. De 2 méternél nagyobb rétegvastagságnál a szín kékessé válik.
Az egész vízmolekula dipol (két ellentétes pólus). A dipolszerkezet alapvetően meghatározza az anyag szokatlan tulajdonságait. A vízmolekula diamágneses.
Egy másik érdekes ingatlan talayavíz: molekulája megszerzi az arany arányának szerkezetét és az anyag szerkezetét - az aranyszelvény arányait. Számos vízmolekula tulajdonsággal rendelkezik a gázfázisban lévő csíkos spektrumok abszorpciójának és emissziójának elemzésével.
Természetes és molekuláris tulajdonságok
Minden anyag, kivéve a vegyi anyagokat, fizikai tulajdonságai vannak a molekuláknak, amelyek bejutnak a szerkezetbe.
A fizikai tudományban a molekulák fogalmát használjáka szilárd anyagok, folyadékok és gázok tulajdonságainak magyarázata. Valamennyi anyag diffúziójára, viszkozitására, hővezető képességére és más tulajdonságaira a molekulák mobilitása határozza meg. Amikor a francia fizikus Jean Perrin tanulmányozta a Brownian mozgást, kísérletileg bizonyította a molekulák létezését. Minden élő szervezet létezik a finom kiegyensúlyozott belső interakciónak köszönhetően. Az anyagok minden kémiai és fizikai tulajdonsága alapvető fontosságú a természettudomány számára. A fizika, a kémia, a biológia és a molekuláris fizika fejlődése egy olyan tudomány létrejöttét szolgálta, mint a molekuláris biológia, feltárva az élet fő jelenségeit.
Statisztikai termodinamikával,A molekuláris spektroszkópia módszerével meghatározott molekulák fizikai tulajdonságai a fizikai kémiában meghatározzák a kémiai egyensúly és a kialakulásuk mértékének kiszámításához szükséges anyagok termodinamikai tulajdonságait.
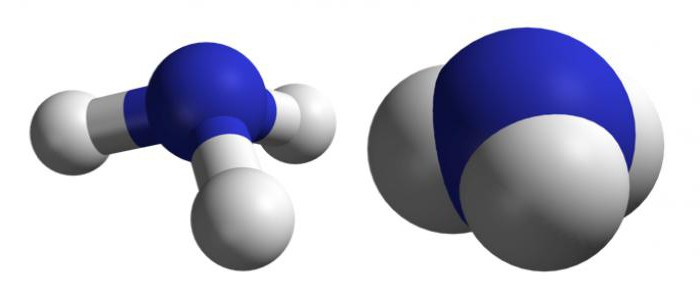
Mi a különbség az atomok és a molekulák tulajdonságai között?
Először is, az atomok nem találhatók szabad állapotban.
A molekuláknak gazdagabb optikai spektrumuk van. Ennek oka a rendszer alsó szimmetriája és a magok új forgásának és oszcillációjának a lehetősége. Egy molekulában a teljes energia három energiából áll, amelyek a komponensek nagyságrendjében különbözőek:
- elektronhéj (optikai vagy ultraibolya sugárzás);
- a magok oszcillációi (a spektrum infravörös része);
- a molekula egészének forgása (rádiófrekvenciás tartomány).
Az atomok jellemző vonali spektrumokat bocsátanak ki, és a molekulák csíkosak, sok, egymástól közeli vonalból állnak.
Spektrális analízis
Optikai, elektromos, mágneses és egyéba molekula tulajdonságait a hullámfüggvényekkel való kapcsolat is meghatározza. A molekulák állapotáról és a köztük való lehetséges átmenetről szóló adatok molekuláris spektrumot mutatnak.
Transzenciák (elektronika) a molekulákbankémiai kötéseket és elektronhéjaik szerkezetét. A nagyobb számú kötésű Spectra hosszú hullámhosszú abszorpciós sávok hullanak a látható tartományba. Ha egy anyag ilyen molekulákból épül fel, akkor jellegzetes színe van. Ezek mind szerves színezékek.
Ugyanazon anyag molekuláinak tulajdonságaiugyanazok az összes aggregációs állapotban. Ez azt jelenti, hogy ugyanazon anyagok esetében a folyékony, gáz halmazállapotú anyagok molekulái nem különböznek a szilárd tulajdonságoktól. Az egyik anyag molekulája mindig ugyanolyan szerkezettel rendelkezik, függetlenül attól, hogy az anyag maga aggregálódik-e.
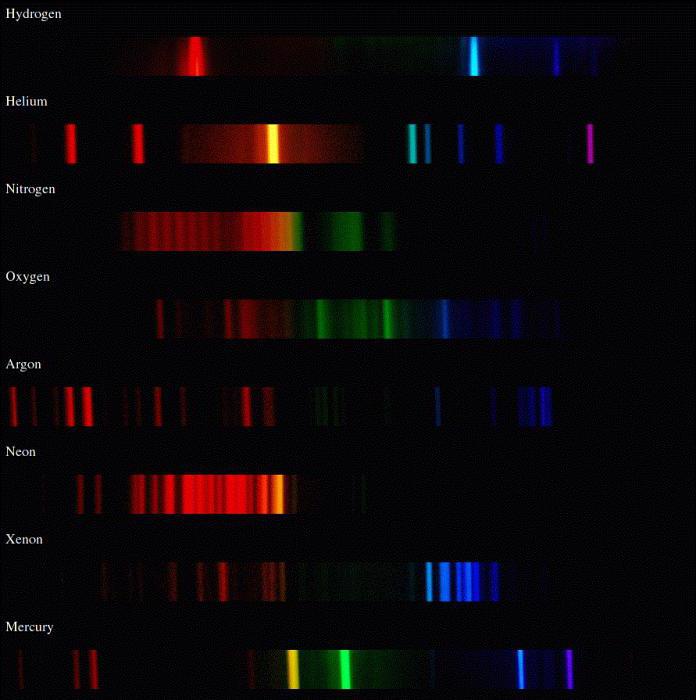
Elektromos jellemzők
Az anyag elektromágneses térben történő viselkedését a molekulák elektromos jellemzői határozzák meg: polarizálhatóság és állandó dipólus pillanat.
A dipólus pillanat a molekula elektromos aszimmetriája. Olyan molekulákban, amelyeknek szimmetriája van, mint a H2nincs állandó dipólus pillanat. A molekula elektronhéjának olyan elektromos mező hatására történő mozgása, amelynek eredményeként egy indukált dipólus pillanat keletkezik benne, a polarizáció. A polarizábilitás és a dipólus pillanatának megtalálásához szükséges a dielektromos állandó mérése.
AC elektromos mező viselkedéseA fény hullámai jellemzik az anyag optikai tulajdonságait, amelyeket az anyag molekulájának polarizálhatósága határoz meg. Közvetlenül összefüggésben áll a polarizabilitással: szóródás, fénytörés, optikai aktivitás és a molekuláris optika egyéb jelenségei.
Gyakran hallja a kérdést: "Mi a molekulák mellett az anyag tulajdonságai függnek?" A válasz nagyon egyszerű.
Az anyagok tulajdonságait - az izometria és a kristályszerkezet mellett - a környezeti hőmérséklet, maga az anyag, a nyomás és a szennyeződések jelenléte határozza meg.

Molekula kémia
Mielőtt egy tudomány létrejött volna, mint a kvantummechanika, a kémiai kötések természete molekulákban megoldatlan rejtély volt. A klasszikus fizika nem tudta megmagyarázni a kötvények irányát és telíthetőségét. Miután megalkotta a kémiai kötés alapelméleti adatait (1927) a legegyszerűbb H2 molekula példáján, az elmélet és a számítási módszerek fokozatosan javulni kezdtek. Például a molekuláris orbitális módszer, a kvantumkémia széles körben elterjedt alkalmazása alapján lehetővé vált a molekulák és kémiai kötések energiájának, az elektronsűrűség eloszlásának és más kísérleti adatoknak egyaránt történő megoszlása.
Ugyanolyan összetételű anyagokat, de eltérő kémiai szerkezetet és különböző tulajdonságokat nevezünk strukturális izomereknek. Különböző szerkezeti képletekkel rendelkeznek, de ugyanazok a molekuláris képletek.
Különféle szerkezeti izomerizmust ismerünk. A különbségek a szénváz szerkezetében, a funkcionális csoport helyzetében vagy a többszörös kötés helyzetében vannak. Továbbá még vannak térbeli izomerek, amelyekben az anyagmolekula tulajdonságait ugyanolyan összetétel és kémiai szerkezet jellemzi. Ezért ugyanazok a szerkezeti és molekuláris formulák. A különbségek a molekula térbeli alakjában rejlenek. A különböző térbeli izomerek képére speciális képleteket használhatunk.
Vannak olyan vegyületek, amelyeket homológoknak neveznek. Struktúrájukban és tulajdonságaikban hasonlóak, de összetételük egy vagy több CH2 csoportban különbözik. A szerkezetben és a tulajdonságokban hasonló összes anyagot homológ sorozatban kombinálják. Miután egy homológ tulajdonságait tanulmányozta, vitathat bármely másról. A homológok halmaza homológ sorozat.
Az anyag kémiai szerkezeteinek átalakításakora molekuláris tulajdonságok drámaian megváltoztak. Példaként említjük még a legegyszerűbb vegyületeket is: a metán, amely még egy oxigénatomot is összekapcsolva, metanol (metil-alkohol - СН3ОН) nevű toxikus folyadékká válik. Ennek megfelelően a vegyi komplementaritás és az élő szervezetekkel szembeni fellépés különbözővé válik. Hasonló, de összetettebb változások következnek be a biomolekulák szerkezetének módosításakor.
A kémiai molekuláris tulajdonságok nagymértékben függeneka molekulák szerkezetétől és tulajdonságaitól: az energia kötéseitől és a molekula geometriájától. Ez különösen a biológiailag aktív vegyületekben rejlik. Melyik versengő reakció dominál, gyakran csak térbeli tényezők határozzák meg, amelyek viszont az eredeti molekuláktól (konfigurációjuktól) függenek. Egy "kényelmetlen" konfigurációjú molekula egyáltalán nem reagál, a másik, ugyanazzal a kémiai összetétellel, de eltérő geometriával reagálhat a reakcióra azonnal.
Számos biológiai folyamata növekedés és a reprodukció során figyelték meg, a reakciótermékek és a kiindulási anyagok geometriai arányai miatt. Tájékoztatásul: a jelentős mennyiségű új gyógyszerek hatása bármely olyan vegyület molekulaszerkezetén alapul, amely biológiailag káros hatással van az emberi szervezetre. A gyógyszer helyettesíti a káros molekulát, és bonyolítja a hatását.
A kémiai képletek segítségével kifejezik a kompozíciót éskülönböző anyagok molekuláinak tulajdonságai. A molekulatömeg alapján kémiai analízist hoztunk létre egy atomi arányt és empirikus képletet állítunk össze.
geometria
A molekula geometriai szerkezetének meghatározásaaz atommagok egyensúlyi elrendezését figyelembe véve. Az atomok kölcsönhatásának energiája az atommagok közötti távolságtól függ. Nagyon nagy távolságokban ez az energia nulla. Amikor az atomok közelednek egymáshoz, kémiai kötés kezdődik. Ezután az atomok erősen vonzódnak egymáshoz.
Ha van egy gyenge vonzás, akkora kémiai kötés kialakulása nem szükséges. Ha az atomok közelebb közelednek egymáshoz, az elektrosztatikus visszataszító erők elkezdenek lépni a magok között. Az atomok erőteljes konvergenciájának akadálya a belső elektronhéjak összeférhetetlensége.
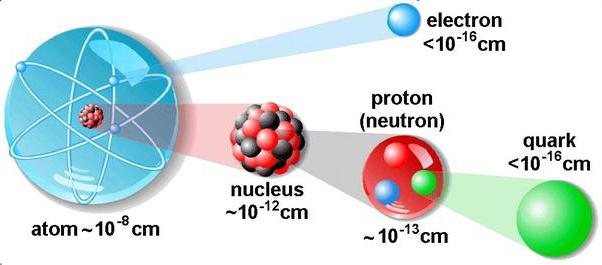
méretek
Nem lehet látni a molekulákat szabad szemmel. Annyira kicsiek, hogy még egy 1000-szeres nagyítású mikroszkóp sem segít nekünk látni őket. A biológusok 0,001 mm-es baktériumot figyeltek meg. De a molekulák több száz és ezerszor kisebbek.
Ma egy bizonyos anyag molekuláinak szerkezetediffrakciós módszerekkel meghatározva: neutronok diffrakciója, röntgen szerkezeti analízis. Van továbbá vibrációs spektroszkópia és elektron paramágneses módszer. A módszer kiválasztása az anyag típusától és állapotától függ.
A molekula mérete feltételes mennyiség, havegye figyelembe az elektronikus héjat. A lényeg az atommagok elektronainak távolsága. Minél nagyobbak, annál kevésbé valószínű, hogy megtalálják a molekula elektronait. A gyakorlatban a molekulák mérete az egyensúlyi távolság mérlegelésével határozható meg. Ez a rés, amelyhez a molekulák maguk is konvergálhatnak, ha szorosan csomagolják egy molekuláris kristályban és egy folyadékban.
Hosszú távolságok pozíciómolekulákatvonzereje, és kicsi, éppen ellenkezőleg, a taszítás. Ezért a molekuláris kristályok röntgensugár-analízise segít megkeresni a molekula méretét. A diffúziós együttható, a gázok hővezető képessége és viszkozitása, valamint az anyag sűrűsége kondenzált állapotban meghatározhatja a molekulatömeg nagyságrendjét.



