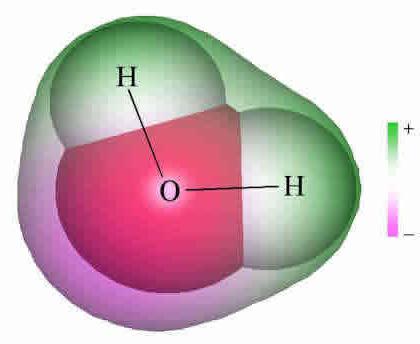
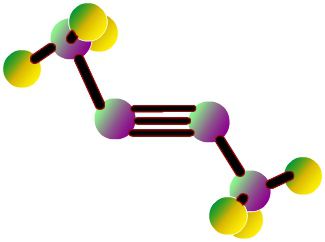
Metán molekuláris és szerkezeti képlete
Molekuláris, szerkezeti és elektronikus képletA metánt Butlerov szervesanyag-szerkezetének elmélete alapján állítják össze. Mielőtt folytatnánk ezeket a képleteket, röviden leírjuk ezt a szénhidrogént.

Metán jellemzői
Ez az anyag robbanásveszélyes, mégisúgynevezett "mocsári" gáz. A végső szénhidrogén különleges illata mindenki számára ismert. Az égés folyamán nem maradnak olyan kémiai összetevők, amelyek negatív hatást gyakorolnak az emberi szervezetre. Ez a metán aktív résztvevője az üvegházhatás kialakulásának.
Fizikai tulajdonságok
Az alkánok homológ sorozatának első képviselőjea tudósok felfedezték a Titan és a Mars légkörében. Tekintettel arra, hogy a metán az élő szervezetek létezésével jár együtt, hipotézis alakult ki az élet létezéséről ezen a bolygón. A Szaturnuszra, Jupiterre, Neptunuszra, Uranusra, a metán a szervetlen eredetű anyagok kémiai feldolgozásának eredményeként jelent meg. A bolygónk felszínén jelentéktelen a tartalom.

Általános jellemzők
A metánnak nincs színe, könnyebb, mint a levegőkétszer, vízben rosszul oldódik. A földgáz összetételében az anyag mennyisége eléri a 98 százalékot. Az olajátadó gáz 30-90% metánt tartalmaz. A metán nagyobb mértékben biológiai eredetű.
A baromfitenyésztők és a tehenek kibocsájtjáka baktériumok gyomrában elég nagy mennyiségű metánt. A homogén alkán-sorozat fontos forrásaik között megkülönböztetjük a mocsarakat, a termeszeket, a földgázszűrést és a növényi fotoszintézis folyamatát. Ha metán nyomot találnak a bolygón, beszélhetünk a biológiai élet létezéséről.

A megszerzés módszerei
A metán részletes szerkezeti képletehogy a molekulájában csak a hibrid felhők által alkotott telített egyszeres kötések szerepelnek. A szénhidrogén előállítására szolgáló laboratóriumi lehetőségek közül megemlítjük a nátrium-acetát szilárd lúgos fúzióját, valamint az alumínium-karbid vízzel való kölcsönhatását.
A metán kékes lánggal ég,Ez kb. 39 MJ / köbméter. Robbanásveszélyes keverékek esetén ez az anyag levegővel képződik. A legveszélyesebb a metán, amelyet az ásványi lelőhelyek föld alatti bányászata során bányákban szabadítanak fel. A szén- és brikettáló dúsító üzemekben, valamint a válogató létesítményekben nagy a kockázata a metán robbanásának.
Fiziológiai hatás
Ha a metán százalékos aránya a levegőben5-16%, az oxigén beáramlása esetén a metán meggyulladhat. Abban az esetben, ha egy vegyi anyag keveréke jelentősen megnő, a robbanás valószínűsége nő.
Ha a levegőben ez az alkán koncentrációja 43 százalék, akkor az fulladás oka.
A robbanás során a propagációs sebesség másodpercenként 500 és 700 méter között van. Miután a metán érintkezik a hőforrással, az alkán meggyulladása néhány késéssel történik.
Ez a tulajdonság a robbanásbiztos elektromos berendezések és a robbanásbiztos robbanóelemek gyártásának alapja.
Mivel a metán a legtermékenyebbstabil, telített szénhidrogén, széles körben alkalmazható ipari és háztartási üzemanyag formájában, és értékes nyersanyagként is használható a kémiai szintézishez. A trietil-metán szerkezeti képlete jellemzi az ilyen típusú szénhidrogének képviselőinek szerkezeti jellemzőit.
A kémiai kölcsönhatás folyamatábanAz ultraibolya besugárzás hatására keletkező klór a reakció több terméke is lehet. A kiindulási anyag mennyiségétől függően klór-metán, kloroform, szén-tetraklorid beszerezhető kicserélés közben.
A metán hiányos égetése esetén korom keletkezik. Katalitikus oxidáció esetén formaldehid keletkezik. A kénnel való kölcsönhatás végterméke szén-diszulfid.

A metán szerkezete jellemzői
Mi a szerkezeti képlet? A metán a (C) általános képletű korlátozó szénhidrogéneket jelentinH2n + 2. Tekintsük egy molekula kialakulásának jellemzőit, hogy megmagyarázzuk, hogyan alakul ki egy szerkezeti képlet.
A metán egy szénatomból és négy hidrogénatomból áll, amelyeket egy kovalens poláris kémiai kötés kapcsol össze. Magyarázzuk meg a szén-szerkezeti képletek szerkezetét.
A hibridizáció típusa
A metán térszerkezetét a következők jellemzik:tetraéderes szerkezet. Mivel a szén külső szintjén négy kondenzációs elektron található, amikor az atom felmelegszik, az elektron áthalad a második s-orbitálistól p. Ennek eredményeképpen az utolsó energia szintjén a szén négy párosítatlan ("szabad") elektron. A metán teljes szerkezeti képlete négy hibrid felhő képződésén alapul, amelyek a térben 109 ° -on 28 percen át irányulnak, ami a tetraéder szerkezetét alkotja. Ezután a hibrid felhők átfedő csúcsai a nem hibrid felhők hidrogénatomjaival fordulnak elő.
A metán teljes és rövidített szerkezeti képleteteljesen megfelel Butlerov elméletének. A szén és a hidrogén között egy egyszerű (egy) kötés keletkezik, így a kémiai reakciókat addíciós reakciók nem jellemzik.
Az alábbiakban a végleges szerkezeti képlet. A metán a telített szénhidrogén osztály első képviselője, jellemzője a végső alkán tipikus tulajdonsága. A metán szerkezeti és elektronikus formája megerősíti a szén szénatom hibridizációját egy adott szerves anyagban.

Az iskolai kémia tanfolyamából
Ez a szénhidrogén-osztály, reprezentatívamely "mocsárgá", a középiskola 10. évfolyamán tanul. Például a gyerekeknek felajánlották a következő karaktert: "Írja le a metán szerkezeti képletét". Meg kell érteni, hogy ezen anyag esetében Butlerov elméletének megfelelően csak kiterjesztett szerkezeti konfiguráció írható le.
A csökkentett képlet egybeesikmolekuláris, CH4 formában kell írni. Az orosz oktatás átszervezésével kapcsolatban bevezetett új szövetségi oktatási normák szerint a kémiai alapoktatás során minden részletesen áttekintésre kerülnek a szerves anyagok osztályainak jellemzőit érintő kérdések.
Ipari szintézis
Alapuló metán, iparimint az acetilén fontos vegyi összetevője. A hő- és elektromos repedések alapja éppen a szerkezeti képlet. A metán ammóniával történő katalitikus oxidáció során hidrociánsavat képez.
Alkalmazza ezt a szerves anyagotszintézisgáz előállítása. A vízgőzzel való kölcsönhatás során szénmonoxid és hidrogén keverékét állítják elő, amely a határérték egyértékű alkoholok, karbonilvegyületek előállításának nyersanyaga.
Különös jelentőséggel bír a nitrogénsavval való kölcsönhatás, ami nitrometánt eredményez.

Alkalmazás autóipari üzemanyag formájában
A természetes források hiánya miattszénhidrogének, valamint a elszegényedés a nyersanyag bázis, akkor válik különösen lényeges kérdés kapcsolódik a keresés az új (alternatív) forrásai az üzemanyag. Az egyik ilyen lehetőség a biodízel, amely metánt tartalmaz.
Tekintettel a benzin közti sűrűség különbségéreaz üzemanyag és az alkán-osztály első képviselője, az autómotorok energiaforrásként való alkalmazásának bizonyos jellemzői vannak. Annak elkerülésére, hogy óriási mennyiségű metánt kell szállítani, a sűrűséget kompresszióval növelni kell (250 atmoszférájú nyomáson). Tárolja a metánt cseppfolyós állapotban az autókba beépített palackokban.
Hatások a légkörre
Már beszéltünk arról, hogy a metán teszihatása az üvegházhatásra. Ha az éghajlati szén-monoxid (4) hatásfokát egy egységre feltételesen veszik, akkor a "mocsári gáz" aránya 23 egység. Az elmúlt két évszázadban a tudósok megfigyelték a metán mennyiségi tartalmának növekedését a Föld légkörében.
Jelenleg a CH becsült száma4 a becslések szerint 1,8 ppm. Annak ellenére, hogy ez a szám 200-szor kisebb, mint a szén-dioxid jelenléte, van egy beszélgetés tudósok közötti a lehetséges beszorulásának által kibocsátott hőt a bolygó.
A "mocsári gáz" kitűnő fűtőértékével kapcsolatban nemcsak a kémiai szintézis végrehajtásában nyersanyagként, hanem energiaforrásként is felhasználták.
Például a metánban különféle gázkazánok, oszlopok vannak kialakítva, amelyek egyéni fűtési rendszerekhez vannak tervezve magánházakban és vidéki házakban.
Az ilyen autonóm fűtési lehetőség nagyon előnyösa lakástulajdonosok számára nem kapcsolódik olyan rendszeres balesetekhez, amelyek központosított fűtési rendszereken fordulnak elő. Az ilyen típusú üzemanyaggal működő gázkazánnak köszönhetően 15-20 perc elég ahhoz, hogy teljesen felmelegítse a kétemeletes házat.

következtetés
Metán, szerkezeti és molekuláris formulákamelyet fent adtak meg, egy természetes energiaforrás. Tekintettel arra, hogy összetételében csak egy szénatom és hidrogénatom van, a környezetvédők elismerik e telített szénhidrogén ökológiai biztonságát.
Normál körülmények között (levegő hőmérséklete 20 ° C, nyomás 101325 Pa), ez az anyag gáz, nem mérgező, vízben oldhatatlan.
A levegő hőmérséklet -161 fokos csökkenése esetén a metán tömörítődik, amelyet széles körben alkalmaznak az iparban.
A metán hatással van az emberi egészségre. Nem mérgező anyag, hanem fulladt gáznak. Vannak még határértékek (MPC) egy adott vegyi anyag tartalmára a légkörben.
Például a bányákban végzett munkák csak azokban engedélyezettekesetben, ha mennyisége nem haladja meg a 300 milliméterenkénti köbmétert. E szerves anyag szerkezetének elemzésével arra a következtetésre juthatunk, hogy a kémiai és fizikai tulajdonságok hasonlóak a telített (korlátozó) szénhidrogén osztály többi képviselőjéhez.
Elemeztük a szerkezeti képleteket, a metán térszerkezetét. A "mocsárgázt" indító homológ sorozat a C általános molekuláris képletével rendelkeziknH2n + 2.